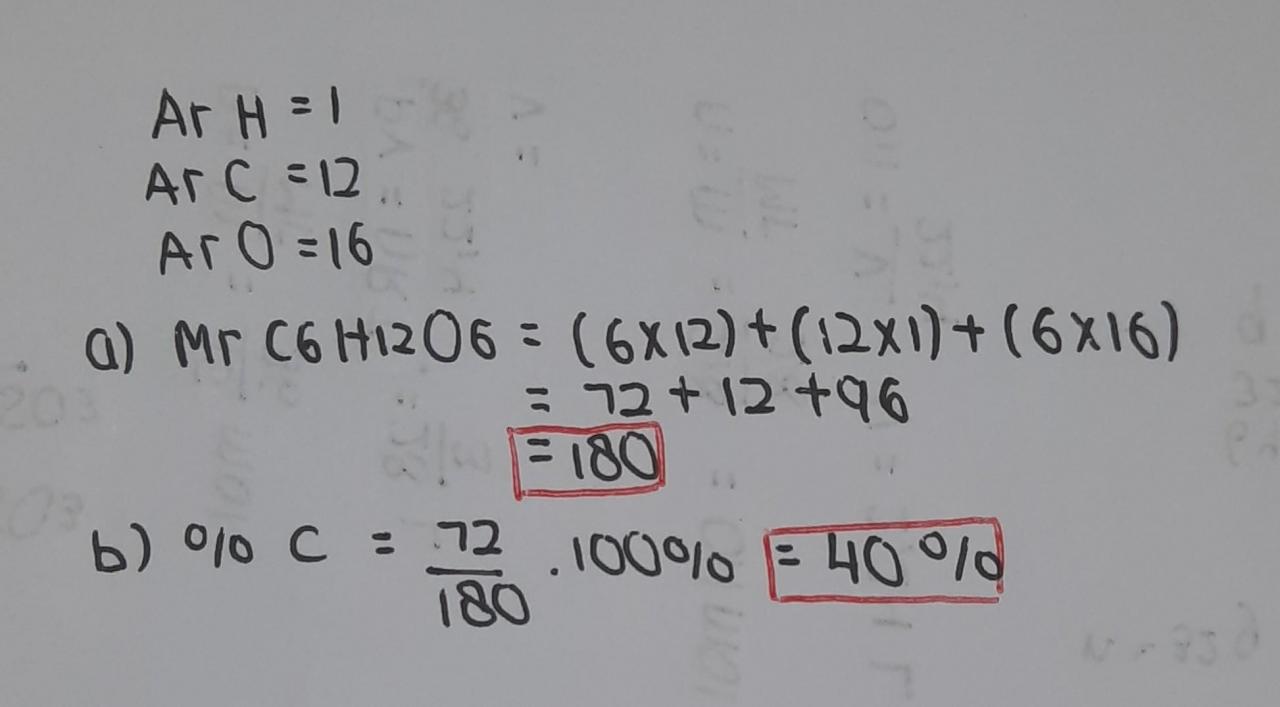
Berapakah jumlah atom n yang terdapat dalam 5 nh4oh adalah ….
Mapel Kimia, Jenjang Sekolah Menengah Pertama
Daftar Isi
↓JAWABAN↓
NH4OH
NH4OHN+ 4(1) + (-2) + (1) = 0
NH4OHN+ 4(1) + (-2) + (1) = 0N+ 3 = 0
Jangan lupa follow
Pertanyaan Baru di Kimia
1. Di ketahui massa atom relatif (Ar) dari H= 1,C=12,0=16. Tentukan A. Mr glukosa (C6H1206)!
B. Persentase massa unsur C dalam senyawa glukosa (C6H1206)!.
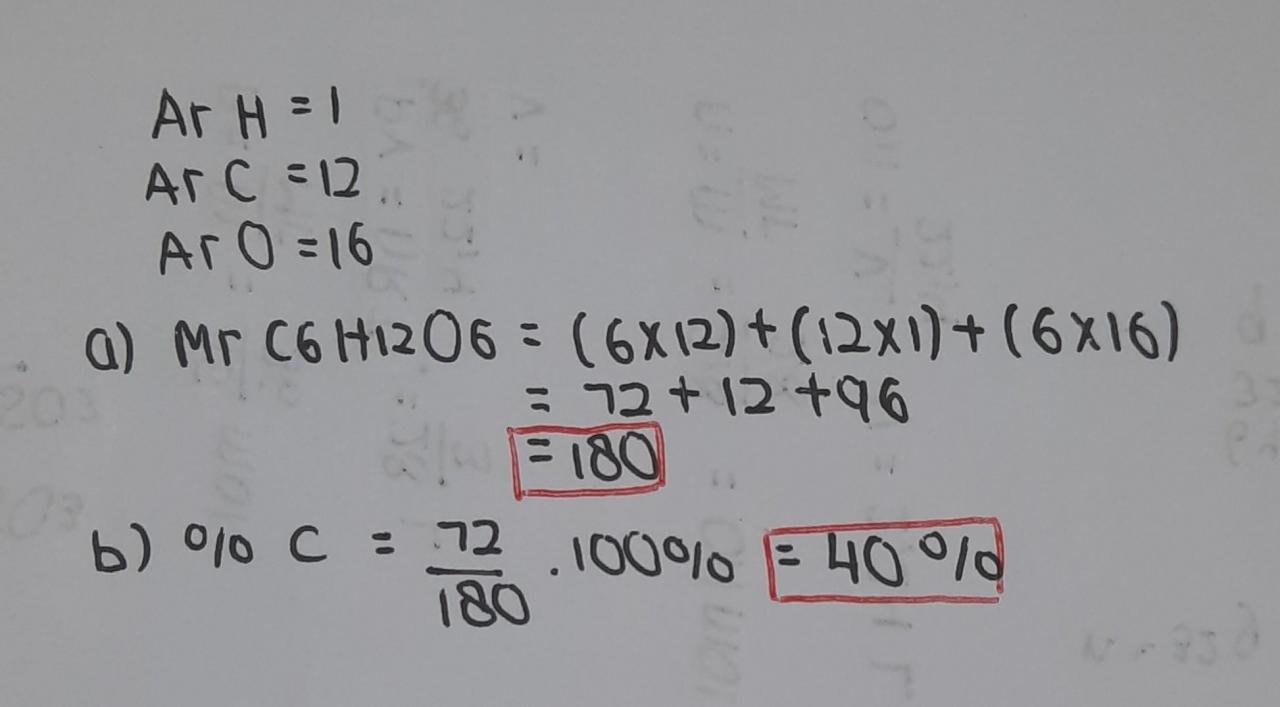
Kimia, Sekolah Menengah Atas
Penyelesaian:
Lihatlah foto yang sudah terlampir
Sebuah viscosimeter distandarkan dengan benzene yang mempunyai koefisien viscositas 0,643 cp, massa jenis 0,879 pada suhu 20 C, waktu alir 183 detik. Waktu alir untuk etanol 378 detik pada 20 C, dengan masssa jenis etanol 0,789. Hitunglah viscositas etanolnya
Kimia, Sekolah Menengah Atas
Sebuah viscosimeter distandarkan dengan benzene yang mempunyai koefisien viscositas 0,643 cp, massa jenis 0,879 g/cm³ pada suhu 20°C, waktu alir 183 detik. Waktu alir untuk etanol 378 detik pada 20°C, dengan masssa jenis etanol 0,789 g/cm³. Viscositas etanolnya adalah 1,192 cp.
_______________________________________________________
Penjelasan
Viskosimeter Ostwald
(kayak praktikum pas kuliah di teknik kimia)
- Persamaan yang dapat digunakan (Pers. Poisseulle) :
- dengan,
η = viskositas (cp)
t = waktu alir (s)
ρ = densitas (g/cm³)
subskrip o = standard (benzene)
Diketahui :
- η₀ = 0,643 cp
t₀ = 183 detik
ρ₀ = 0,879 g/cm³ - η = ? cp
t = 378 detik
ρ = 0,789 g/cm³
Penyelesaian
_______________________________________________________
Pelajari lebih lanjut
- Materi tentang prinsip kerja viskosimeter :
- Materi tentang rumus koefisien viskositas :
- Materi tentang etanol :
_______________________________________________________
Detail jawaban
Mapel : Kimia
Kelas : XII
Bab : Senyawa Karbon – Senyawa Turunan Alkana
Kode : 12.7.5
(Kalau bisa dipermudah, kenapa harus dipersulit) – RoyAlChemi
#KIMIA_ITU_ASYIK #Belajar_Bersama_Brainly
Larutan yang termasuk golongan asam kuat adalah …. A. HC1, H₂S, H₂SO4 B. HBr, CH₂COOH, H₂CO3 C. HNO3, HCl, H₂SO4 D. H3PO4, H3PO3, H₂S E. HNO3, HI, HF
Kimia, Sekolah Menengah Atas
Jawaban : C.( HN03, HCI, H2SO4)
Penjelasan:
yang termasuk golongan asam kuat termasuk:
Asam perklorat (HClO4) , Asam bromida (HBr), Asam hidrogen iodida (HI), Asam klorida (HCl), Asam nitrat (HNO3), Asam sulfat (H2SO4), Asam klorat (HClO3)
1. Perhatikan skema dogma sentral informasi genetik berikut. Pertanyaan: Berdasarkan skema diatas: (a) Jelaskan skema dogma sentral tersebut secara singkat dan tepat! (b) Jelaskan dengan singkat proses transkripsi dan translasi dalam pembentukan protein secara umum. (c) Apa yang terjadi pada proses translasi dalam sintesis protein jika mRNA tidak menyandikan triplet UAA, UAG atau UGA? Jelaskan pula dampaknya terhadap kesehatan tubuh manusia.
Jawab :
a. Dogma sentral menjelaskan mengenai proses perubahan gen dari DNA menjadi RNA, dan RNA menjadi protein. Dogma ini menjelaskan bagaimana proses pembacaan materi genetik menjadi protein yang berperan di setiap tahap metabolisme di dalam tubuh suatu organisme. Berdasarkan skema diatas terlihat bahwa dogma sentral terdiri dari tiga tahap yaitu replikasi, transkripsi dan translasi. Tahap replikasi dilakukan untuk memasok DNA pada setiap organisme, sedangkan tahap transkripsi bertujuan untuk menulis ulang DNA dalam bentuk mRNA (messenger RNA). Tahap translasi untuk menterjemahkan mRNA tersebut menjadi suatu protein.
Kimia, Sekolah Menengah Atas
- Proses transkripsi: RNA polimerase akan memisahkan untaian DNA menjadi dua di dalam nukleus dengan cara bergerak dari terminator menuju promoter. Setelah RNA polimerasesampai di promoter (inisiasi), maka proses selanjutnya disebut dengan elongasi, yaitu RNA polimerase akan kembali ke terminator dan membentuk mRNA. Pada saat RNA polimerase dan mRNA sampai diterminator (terminasi) maka proses transkripsi selesai.
- Proses translasi: pada inisiasi, kodon pertama mRNA yang bertemu dengan ribosom disebut dengan kodon start, yaitu kodn AUG. pada tahap elongasi, kodon yang dibawa oleh mRNA akan diterjemahkan menjadi asam amino dan setiap asam amino akan digabungkan oleh tRNA menjadi rantai polipeptida. pada tahaan terminasi proses translasi berhenti setelah salah satu kodon stop bertemu dengan ribosom.
- Peristiwa yang terjadi apabila proses translasi dalam sintesis protein jika mRNA tidak menyandikan triplet UAA, UAG atau UGA adalah terbentuknya jenis protein yang berbeda sehingga menimbulkan mutasi gen pada makhluk hidup, contohnya yaitu anemia sickle cell.
Pembahasan:
Sintesis protein .merupakan proses terbentuknya protein dalam tubuh yang dilakukan oleh RNA berdasarkan adanya perintah dari atau kode DNA. Sintesis protein terjadi di dalam nukleus (inti sel) dan ribosom.
Pelajari lebih lanjut
Pelajari lebih lanjut mengenai materi sintesis protein pada link
#BelajarBersamaBrainly
#SPJ1
Jika 15 gram senyawa karbon (Mr = 120) dibakar sempurna, akan menghasilkan 22 gram karbon dioksida dan 9 gram air (Ar O = 16, C =12, H =1). Rumus molekul senyawa karbon tersebut adalah
adalah…
A. C2H4O2 D. C4H10O2
B. C2H6O2 E. C4H8O4
C. C3H6O3
Kimia, Sekolah Menengah Atas
Jika 15 gram senyawa karbon (Mr = 120) dibakar sempurna, akan menghasilkan 22 gram karbon dioksida dan 9 gram air (Ar O = 16, C =12, H =1). Rumus molekul senyawa karbon tersebut adalah C₄H₈O₄.
Opsi E.
—————————————————————————————————-
Penjelasan dengan langkah-langkah
Diketahui :
- Mr senyawa karbon = 120
- m CO₂ = 22 g
- m H₂O = 9 g
- Ar O = 16
- Ar C = 12
- Ar H = 1
Ditanyakan :
Rumus molekul senyawa karbon = ?
Penyelesaian :
Menghitung Mr CO₂ dan H₂O
- Mr CO₂ = Ar C + 2 x Ar O
Mr CO₂ = 12 + 2 x 16
Mr CO₂ = 44 g/mol - Mr H₂O = 2 x Ar H + Ar O
Mr H₂O = 2 + 16
Mr H₂O = 18 g/mol
Menghitung mol CO₂ dan H₂O hasil
- Mol CO₂ = massa : Mr
Mol CO₂ = 22 g : 44 g/mol
Mol CO₂ = 0.5 mol - Mol H₂O = massa : Mr
Mol H₂O = 9 + 18
Mol H₂O = 0.5 mol
Menghitung massa atom C, H, dan O dalam senyawa karbon
- Massa atom C dalam senyawa karbon
CO₂ ==> C⁴⁺ + 2O²⁻
m C = mol CO₂ x Ar C
m C = 0.5 x 12
m C = 6 gram - Massa atom H dalam senyawa karbon
H₂O ==> 2H⁺ + O²⁻
m H = 2 x mol H₂O x Ar H
m H = 2 x 0.5 x 1
m H = 1 gram - Massa atom O dalam senyawa karbon
m senyawa = m O + m H + m C
m O = m senyawa – m H – m C
m O = 15 – 1 – 6
m O = 8 gram
Perbandingan atom C, H, dan O dalam senyawa karbon
- mol C : mol H : mol O = m C / Ar C : m H / Ar H : m O / Ar O
mol C : mol H : mol O = 6/12 : 1 : 8/16
ketiga angka dibagi 0.5, menjadi
mol C : mol H : mol O = 1 : 2 : 1 - Jadi rumus empiris senyawa karbon = CH₂O
Penentuan rumus molekul
- Mr senyawa karbon = n x Mr senyawa karbon dari rumus empiris
120 = n x (1 x Ar C + 2 x Ar H + 1 x Ar O)
120 = n x (1 x 12 + 2 x 1 + 16)
120 = n x 30
n = 120 : 30 = 4 - Jadi rumus molekul senyawa :
(CH₂O)₄ atau C₄H₈O₄
—————————————————————————————————-
Pelajari lebih lanjut
- Materi tentang rumus empiris dan rumus molekul :
- Materi tentang penentuan rumus molekul senyawa karbon :
- Materi tentang penentuan rumus molekul dari CxHyOz :
—————————————————————————————————-
Detail jawaban
Mapel : Kimia
Kelas : XII
Bab : Senyawa karbon dan reaksi identifikasi
Kode : 12.7.8





