
Tentukan rumus umum dari senyawa alkana‚ alkena dan alkuna‚ kemudian tentukan rumus molekul dari senyawa yang memiliki harga: A.n = 4 (alkana)
B.n = 17 (alkana)
C.n = 13 (alkena)
D.n = 25 (alkena)
E.n = 5 (alkuna)
F.n = 48 (alkuna)
Jawab semua ya
Mapel Kimia, Jenjang Sekolah Menengah Atas
Penjelasan:
rumus alkana : CnH2n+2
rumus alkena : CnH2n
rumus alkuna : CnH2n-2
a. C4H10
b. C17H36
c. C13H26
d. C25H50
e C5H8
f. C48H94
kalo benar kasih jawaban terbaik ya hehe
Daftar Isi
Pertanyaan Baru di Kimia
Ph suatu larutan jika diukur dengan phmeter adalah 8,7. sifat larutan tersebut adalah …
Kimia, Sekolah Menengah Pertama
Jawaban:
basa
Penjelasan:
ph <7 asam
ph =7 netral
ph >7 basa
Mohon pencerahan nya

Kimia, Sekolah Menengah Atas
Jawaban:
Menghitung Mr K2SO4
Mr K2SO4 = ( 2 x Ar K ) + ( 1 x Ar S ) + ( 4 x Ar O )
( 2 x 39 ) + ( 1 x 32 ) + ( 4 x 16 ) = 174
Menghitung mol K
massa K = n x Ar K
3,9 = n x 39
n = 0,1 mol
Menghitung mol K2SO4 dengan perbandingan koefisien:
Koefisien K : K2SO4 = 1 : 1 jadi mol K2SO4 = 0,1 mol
Menghitung massa K2SO4
massa K2SO4 = n x Mr
0,1 mol x 174 = 17,4 gram
Jawaban:
Berikut caranya ya
Semoga membantu 🙂
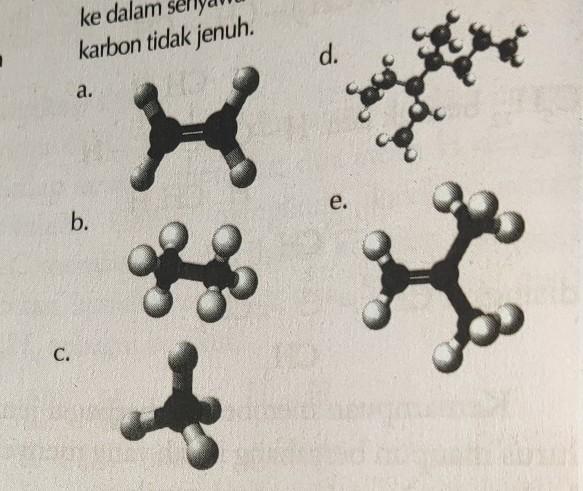
Kelompokkan struktur senyawa karbon berikut ke dalam senyawa karbon jenuh atau senyawa karbon tidak jenuh.
Kimia, Sekolah Menengah Atas
Penjelasan:
penentuan senyawa karbon jenuh dan tak jenuh ditentukan berdasarkan ikatan yang ada di dalam strukturnya. apabila hanya memiliki ikatan tunggal (alkana) maka disebut senyawa karbon jenuh. sedangkan apabila memiliki ikatan rangkap (alkena dan alkuna) maka disebut senyawa karbon tak jenuh.
pada gambar, senyawa a dan e memiliki ikatan rangkap sehingga disebut senyawa karbon tak jenuh
sedangkan b,c, dan d hanya memiliki ikatan tunggal maka disebut senyawa karbon jenuh
Q. Chemistry soal terlampir diatas
Note 1 : jawab pakai penjelasan, yang mau request silahkan!
Note 2 : silahkan request dari user berbeda hingga 10 soal, user yang sama gak boleh request lagi!

Kimia, Sekolah Menengah Atas
Jawaban:
Tertera di penjelasan
Penjelasan:
a. Kw = [H+] [OH-]
Kw = tetapan ionisasi air pada suhu 25°C = 1 x 10^-14
maka [OH-] = Kw / [H+]
[OH-] = 10^-14 / 7,5 x 10^-3
[OH-] = 0,133 x 10^-11 M atau 1,33 x 10^-12 M
b. Karena [H+] > [OH-] maka air limbah tersebut bersifat asam
Sebanyak 50 ml larutan CH3COOH 0,2 m (ka=10⁵) dicampurkan dengan 50 ml larutan NaOH 0.1 m. Hilunglah pH larutan tersbt
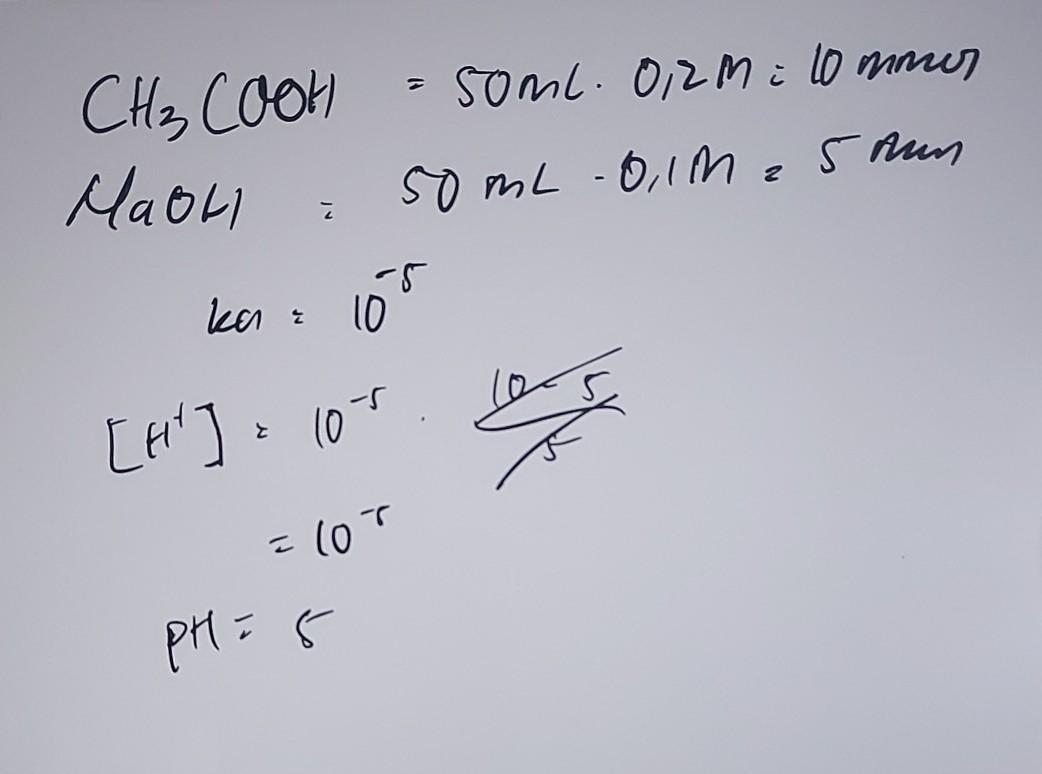
Kimia, Sekolah Menengah Atas
jawabannya ada pada gambar di atas



