Jika Volume1 mol gas C2H2 diukur pada kondisi STP ( T = 00C , P = 1 atm) = 22,4 liter , maka harga 0,1 mol gas C2H2 adalah. .
Mapel Kimia, Jenjang Sekolah Menengah Atas
Jawaban:
2,24 L
Penjelasan:
V C2H2 pada keadaan STP = n x 22,4 L/mol
V C2H2 pada keadaan STP = 0,1 mol x 22,4 L/mol
V C2H2 pada keadaan STP = 2,24 L
Daftar Isi
Pertanyaan Baru di Kimia
100 gram C3H8 direaksikan sempurna dengan 100 gram O2, hitung jumlah massa gas-gas hasil reaksi. Bila Ar C=12, H=1, O= 16 (gram/mol)
Kimia, Sekolah Menengah Atas
Jawaban:
massa CO2 : 83,16 gram
massa H2O : 45,36 gram
Penjelasan:
pembakaran hidrokarbon selalu menghasilkan CO2 dan H2O
C3H8 + O2 —–> CO2 + H2O
setarakan reaksinya sehingga menjadi
C3H8 + 5O2 —-> 3CO2 + 4H2O
hitung mol mula-mula masing2 pereaksi
mol : massa/Mr
mol C3H8 : 100/44 = 2,27 mol
mol O2 : 100/32 = 3,13 mol
C3H8 + 5O2 ——> 3CO2 + 4H2O
m 2,27. 3,13
b. 0,63 3,13. 1,89. 2,52
s. 1,64. -. 1,89. 2,52
sehingga mol CO2 dan H2O yang dihasilkan berturut2 adalah 1,89 dan 2,52 mol
massa CO2:
massa = mol . Mr
= 1,89 . 44
= 83,16 gram
massa H2O
massa = mol . Mr
= 2,52 . 18
= 45,36 gram
kalo benar kasih jawaban terbaik, kalo salah komen:)
Massa molekul relatif (mr) co(nh2)2, jika diketahui (ar c = 12, h = 1, n=14 dan o = 16) adalah ….
Kimia, Sekolah Menengah Pertama
Penjelasan:
mr=(a×(ar c)+a×(ar o)+a×(ar n)+a×(ar h))
mr=(12(1)+16(1)+14(2)+1(4))
mr=(12+16+28+4)
mr=60
keterangan
a= jumlah atom dalam senyawa
Tentukan rumus umum dari senyawa alkana‚ alkena dan alkuna‚ kemudian tentukan rumus molekul dari senyawa yang memiliki harga: A.n = 4 (alkana)
B.n = 17 (alkana)
C.n = 13 (alkena)
D.n = 25 (alkena)
E.n = 5 (alkuna)
F.n = 48 (alkuna)
Jawab semua ya
Kimia, Sekolah Menengah Atas
Penjelasan:
rumus alkana : CnH2n+2
rumus alkena : CnH2n
rumus alkuna : CnH2n-2
a. C4H10
b. C17H36
c. C13H26
d. C25H50
e C5H8
f. C48H94
kalo benar kasih jawaban terbaik ya hehe
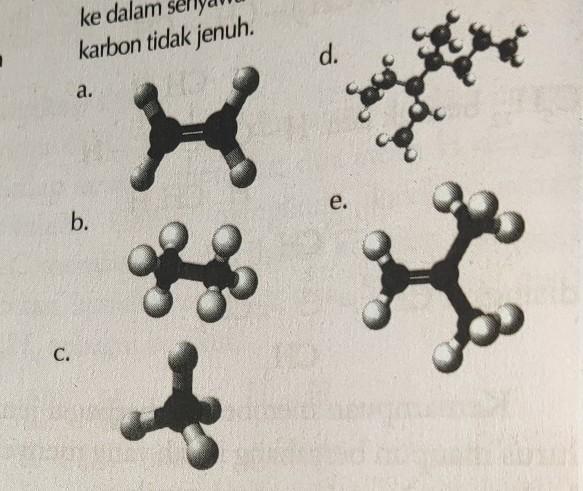
Kelompokkan struktur senyawa karbon berikut ke dalam senyawa karbon jenuh atau senyawa karbon tidak jenuh.
Kimia, Sekolah Menengah Atas
Penjelasan:
penentuan senyawa karbon jenuh dan tak jenuh ditentukan berdasarkan ikatan yang ada di dalam strukturnya. apabila hanya memiliki ikatan tunggal (alkana) maka disebut senyawa karbon jenuh. sedangkan apabila memiliki ikatan rangkap (alkena dan alkuna) maka disebut senyawa karbon tak jenuh.
pada gambar, senyawa a dan e memiliki ikatan rangkap sehingga disebut senyawa karbon tak jenuh
sedangkan b,c, dan d hanya memiliki ikatan tunggal maka disebut senyawa karbon jenuh
Massa 5 mol fecl3 dengan jika ar fe= 56 dan cl = 35.5 adalah
Kimia, Sekolah Menengah Pertama
Penjelasan:
g=mol×mr
g=5×(56+3(35.5))
g=812,5 gram



